Naukowcy z Małopolskiego Centrum Biotechnologii Uniwersytetu Jagiellońskiego, kierowani przez dr Antoninę Naskalską, stworzyli innowacyjną nanocząstkę, która może stanowić odpowiedź na jedno z najpoważniejszych wyzwań współczesnej immunologii – konieczność szybkiego reagowania na pojawiające się patogeny, w tym nowe warianty wirusów, np. SARS-CoV-2. W odróżnieniu od klasycznych szczepionek, które wymagają czasochłonnych procesów opracowywania i testowania, nanocząstka ta została zaprojektowana w sposób modułowy, umożliwiający szybką wymianę zarówno antygenów, jak i stymulantów układu odpornościowego.
Czytaj też: Jedna szczepionka, by ochronić przed wszystkimi wirusami
Podstawą projektu jest kapsyd fagowy – naturalna osłonka białkowa wirusów infekujących bakterie – pozbawiony własnego materiału genetycznego, a więc niezdolny do namnażania. W tej formie kapsyd staje się bezpiecznym i elastycznym nośnikiem, który naukowcy “uzbroili” w białko RBD koronawirusa, występujące w formie trymerycznej – takiej samej, jak w realnym patogenie. To kluczowe dla skutecznego naśladowania struktury wirusa i wywołania silnej odpowiedzi immunologicznej.
Uniwersalna szczepionka coraz bliżej? Tak bardzo jej potrzebujemy
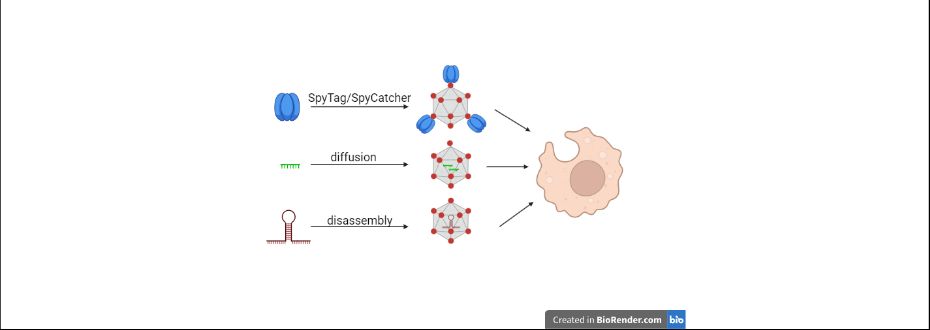
Nowa nanocząstka działa jak biologiczny kameleon – jej powierzchnia może zostać szybko “przeprogramowana”, by prezentować antygeny charakterystyczne dla różnych wirusów, nie tylko koronawirusa, ale potencjalnie także grypy, RSV, czy nowych patogenów zoonotycznych. Zastosowany system wiązań SpyTag/SpyCatcher pozwala na stabilne i ukierunkowane mocowanie trymerycznych białek na powierzchni kapsydu, co znacząco zwiększa ich immunogenność.
Czytaj też: Nowa szczepionka usuwa ślady raka trzustki. Początek końca śmiertelnej diagnozy
Zespół UJ poszedł jednak o krok dalej. Do wnętrza kapsydu, niczym do miniaturowego kontenera, wprowadzono cząsteczki mogące pełnić rolę adjuwantów, czyli wzmacniaczy odpowiedzi odpornościowej – krótkie fragmenty jednoniciowego DNA lub dłuższe sekwencje kodującego mRNA. To połączenie funkcji – powierzchniowej prezentacji antygenów i wnętrznego dostarczania immunostymulantów – czyni z nanocząstki wysoce wydajny nośnik szczepionkowy nowej generacji.
Aby potwierdzić, że prezentowane na powierzchni kapsydu białka rzeczywiście przyjmują formę zbliżoną do tej występującej w aktywnym wirusie, naukowcy skorzystali z techniki kriogenicznej mikroskopii elektronowej, przeprowadzonej w Narodowym Centrum Promieniowania Synchrotronowego SOLARIS. To właśnie tam udało się zwizualizować trójwymiarowy układ trymerycznego RBD i potwierdzić, że projektowana struktura spełnia wymagania biologiczne niezbędne do efektywnej prezentacji antygenu układowi odpornościowemu.
Kriomikroskopia pozwala nie tylko “zajrzeć” do wnętrza nanocząstki z niespotykaną wcześniej rozdzielczością, ale także dokumentować jej przestrzenną konfigurację. Dzięki temu potwierdzono, że prezentowany model ma realny potencjał do skutecznego działania jako szczepionka.
Wyniki projektu zostały opublikowane w czasopiśmie International Journal of Pharmaceutics. Wśród współautorów oprócz dr Naskalskiej znaleźli się Marta Walczak, Agnieszka Dąbrowska, dr inż. Michał Bochenek, dr hab. Artur Biela, prof. UJ oraz prof. Jonathan Heddle – znany z badań nad białkami syntetycznymi i nanostrukturami molekularnymi. Projekt mógł zostać zrealizowany dzięki finansowaniu Narodowego Centrum Nauki oraz wsparciu Ministerstwa Nauki i Szkolnictwa Wyższego, w ramach programu wykorzystania infrastruktury badawczej SOLARIS.
Co dalej?
Choć opracowana nanocząstka to na razie prototyp testowany na modelowych komórkach in vitro, wyniki są obiecujące. Potwierdzono, że komórki układu odpornościowego reagują na jej obecność, co otwiera drogę do dalszych badań na zwierzętach, a w przyszłości – do badań klinicznych. Elastyczność, bezpieczeństwo i potencjał szybkiego dostosowania czynią z niej obiecującą alternatywę wobec obecnych platform szczepionkowych, w tym technologii mRNA czy wektorów adenowirusowych.
Co więcej, rozwiązanie UJ może znaleźć zastosowanie nie tylko w walce z pandemią, ale również w przygotowaniach do tzw. choroby X – nieznanego jeszcze patogenu, który może wywołać kolejną globalną epidemię. Mając gotowy system nośnikowy, który można w krótkim czasie uzbroić w dowolny antygen i adjuwant, społeczność naukowa zyskuje przewagę nad przyszłymi kryzysami zdrowotnymi.
