Drobnokomórkowy rak płuc od lat stanowi jedno z największych wyzwań współczesnej onkologii. Szybko rośnie, wcześnie daje przerzuty i niemal zawsze wraca po leczeniu, odbierając pacjentom szanse na długotrwałe przeżycie. Teraz naukowcy z Hospital del Mar Research Institute w Barcelonie, we współpracy z hiszpańską siecią CIBERONC, odkryli, że dodanie inhibitora genu MET do standardowej immunochemioterapii może odwrócić niekorzystne mikrośrodowisko guza, przywrócić skuteczność układu odpornościowego i w części przypadków doprowadzić do całkowitej regresji nowotworu. Wyniki, opublikowane w Cell Reports Medicine, otwierają nowy rozdział w walce z jednym z najbardziej śmiertelnych nowotworów człowieka.
Drobnokomórkowy rak płuc nie daje zbyt wiele czasu na interwencję
Choć odpowiada tylko za ok. 13-20 proc. wszystkich przypadków raka płuc, drobnokomórkowy rak płuc (SCLC) jest odpowiedzialny za nieproporcjonalnie dużą liczbę zgonów. Jego trzyletni wskaźnik przeżycia wynosi zaledwie 15 proc. Dzieje się tak, ponieważ choroba rozwija się wyjątkowo szybko, a moment diagnozy często przypada na stadium, w którym przerzuty obejmują już liczne narządy i wykluczają interwencję chirurgiczną. Komórki SCLC dzielą się błyskawicznie, a nowotwór charakteryzuje się wyjątkową zdolnością do wytwarzania oporności na leczenie – zarówno na leki cytotoksyczne, jak i na immunoterapię.
Czytaj też: Jak leczymy raka płuca w Polsce? Eksperci potwierdzają: potencjał mamy, ale czas ucieka
Obecny standard obejmuje skojarzenie chemioterapii opartej na pochodnych platyny i etopozydzie z immunoterapią wykorzystującą przeciwciała anty-PD-L1. Takie leczenie potrafi na początku zahamować rozwój choroby, jednak niemal zawsze następuje nawrót, często w ciągu kilku miesięcy, a kolejne linie leczenia są zwykle mało skuteczne.
U podstaw tej wyjątkowej agresywności leżą m.in. zaburzenia w szlaku sygnałowym HGF/MET. MET to receptor kinazy tyrozynowej zlokalizowany na powierzchni komórek, który aktywuje się po związaniu z HGF, czyli czynnikiem wzrostu hepatocytów. W zdrowych tkankach szlak HGF/MET bierze udział w procesach regeneracyjnych i rozwoju embrionalnym, stymulując proliferację, migrację oraz przeżycie komórek. Jednak w przypadku nowotworów mechanizm ten ulega patologicznej deregulacji.
W SCLC nadekspresja MET – obserwowana u około połowy pacjentów – prowadzi do ciągłej aktywacji kaskad sygnałowych takich jak PI3K-AKT, RAS-MAPK czy STAT3. Skutkiem jest nie tylko przyspieszony cykl komórkowy i nasilenie angiogenezy, ale także głębokie przeobrażenie mikrośrodowiska guza. Pod wpływem MET środowisko to staje się “zimne” immunologicznie – praktycznie pozbawione aktywnych limfocytów cytotoksycznych CD8+, a jednocześnie wypełnione komórkami supresorowymi, takimi jak makrofagi M2 czy MDSC, które hamują odpowiedź immunologiczną i chronią nowotwór przed destrukcją. W takim otoczeniu nawet nowoczesne terapie immunologiczne, w tym przeciwciała anty-PD-L1, nie są w stanie zainicjować skutecznego ataku układu odpornościowego.
Genetyczna pięta achillesowa nowotworu
Zespół dr Edurne Arrioli, szefowej sekcji raka płuca w Hospital del Mar i badaczki CIBERONC, postanowił sprawdzić, czy zablokowanie MET może przełamać tę barierę. W modelach mysich SCLC przeprowadzono porównanie czterech schematów leczenia: brak terapii, sama chemioterapia, połączenie chemioterapii z immunoterapią anty-PD-L1 oraz trójkombinacja obejmująca chemioterapię, immunoterapię i inhibitor MET.
Czytaj też: Nie tylko rak płuca, nerki czy czerniak. Immunoterapia pomaga także w leczeniu tych nowotworów
Efekty okazały się spektakularne. W grupie otrzymującej inhibitor MET wraz z immunochemioterapią sześć z dziewięciu guzów całkowicie zniknęło, a pozostałe rosły wolniej niż w jakimkolwiek innym schemacie. Analiza przeżycia wykazała, że myszy z tej grupy żyły znacząco dłużej.
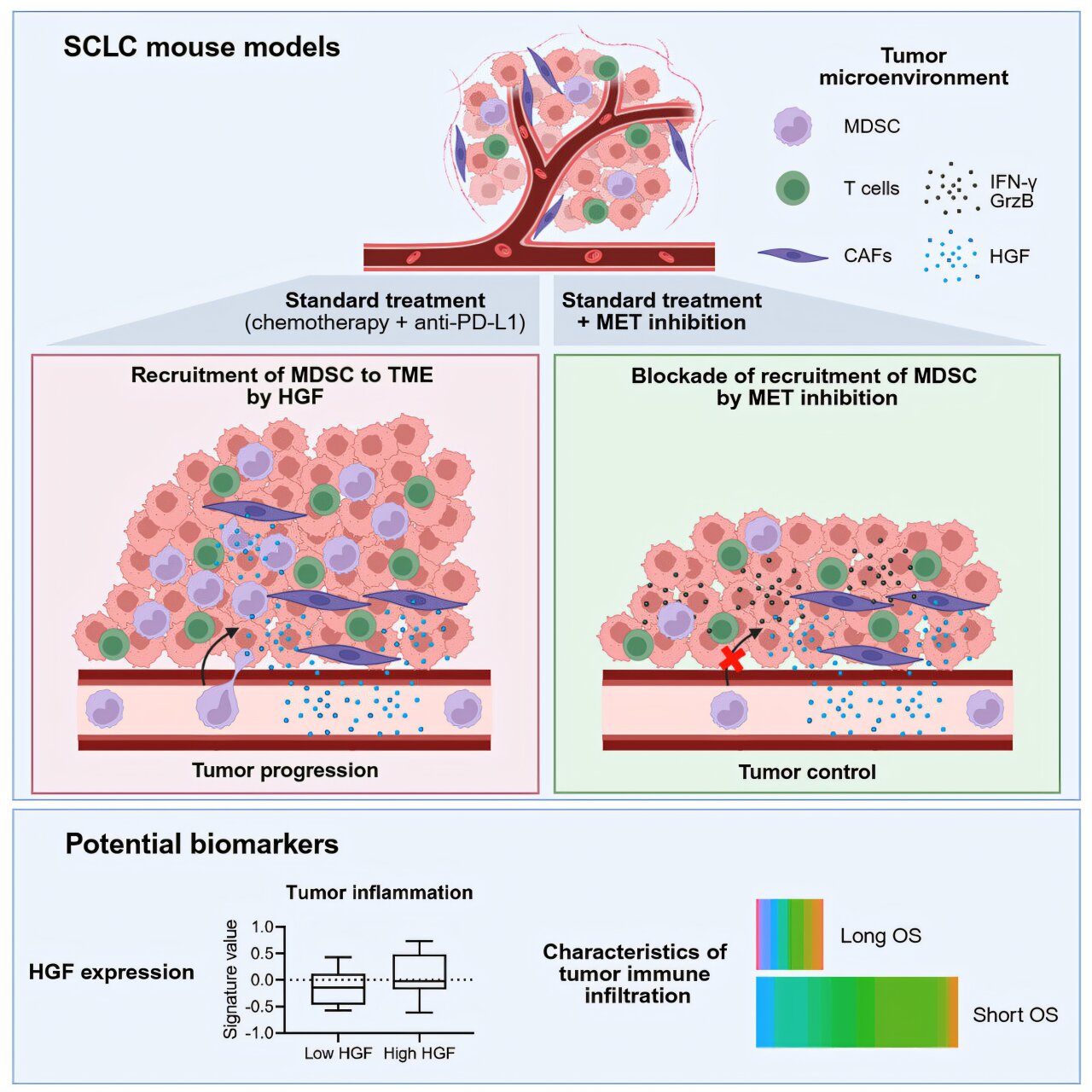
Inhibitor MET nie niszczy komórek nowotworowych bezpośrednio, lecz modyfikuje środowisko, w którym one funkcjonują. Zablokowanie receptora MET prowadzi do spadku aktywności sygnałowej promującej immunosupresję. Zmienia się profil wydzielanych w obrębie guza cytokin – maleje produkcja czynników sprzyjających rekrutacji komórek supresorowych, a rośnie poziom prozapalnych molekuł, takich jak interferon gamma czy interleukina 2. Mikrośrodowisko staje się bardziej “gorące” immunologicznie, co oznacza, że aktywowane przez immunoterapię limfocyty T mogą swobodniej wnikać do guza, rozpoznawać komórki nowotworowe i je niszczyć.
Co istotne, badanie wykazało, że MET wpływa nie tylko na skuteczność immunoterapii, ale także na wrażliwość guza na chemioterapię. Nadaktywność MET wydaje się chronić komórki rakowe przed cytotoksycznym działaniem leków, a jej blokowanie przywraca podatność na klasyczne cytostatyki.
Aby zweryfikować, czy obserwacje z modeli zwierzęcych mają odzwierciedlenie w ludzkiej chorobie, naukowcy przeanalizowali próbki guzów od pacjentów z SCLC. Okazało się, że wysoki poziom MET koreluje z gorszym rokowaniem, niższą liczbą limfocytów T w guzie oraz większą opornością zarówno na chemioterapię, jak i immunoterapię. Te same cechy mikrośrodowiska – dominacja komórek supresorowych, słaba infiltracja przez komórki efektorowe – obserwowano zarówno w próbkach ludzkich, jak i w modelach mysich, co dodatkowo potwierdza zasadność nowego podejścia terapeutycznego.
Perspektywa kliniczna
Badacze podkreślają, że wyniki są kulminacją ponad dekady pracy nad zrozumieniem roli MET w SCLC. Kolejnym krokiem będzie badanie kliniczne, w którym inhibitor MET zostanie włączony po zakończeniu początkowej fazy leczenia immunochemioterapią, w ramach terapii podtrzymującej opartej na samej immunoterapii. Celem będzie sprawdzenie, czy taka strategia może wydłużyć okres kontroli choroby i opóźnić lub zapobiec nawrotowi.
Jeżeli efekty przedkliniczne zostaną potwierdzone w badaniach z udziałem pacjentów, inhibitor MET może stać się brakującym elementem skutecznej terapii drobnokomórkowego raka płuc, a poziom ekspresji MET – kluczowym biomarkerem pomagającym wybrać optymalny schemat leczenia. To przykład tego, jak celowanie w molekularne mechanizmy odporności guza, a nie tylko w same komórki nowotworowe, może otworzyć zupełnie nowe możliwości w onkologii.
