Od odkrycia morfiny w XIX wieku opioidy stały się fundamentem leczenia silnego bólu. Ich mechanizm – wiązanie z receptorami μ-opioidowymi w ośrodkowym układzie nerwowym – pozwala skutecznie tłumić przewodzenie sygnałów bólowych. Niestety, ta sama droga odpowiada za szereg efektów ubocznych, od spowolnienia oddychania po silne uzależnienie psychiczne i fizyczne.
Czytaj też: Przełom po 25 latach. Europa blisko zatwierdzenia leku na glejaka
W Stanach Zjednoczonych liberalna polityka przepisywania leków takich jak OxyContin na przełomie lat 90. i 2000. doprowadziła do epidemii nadużywania opioidów, która szybko przekształciła się w kryzys fentanylowy. Według danych CDC w 2023 r. z powodu przedawkowania opioidów zmarło ponad 80 tys. osób. Problem narasta również w Kanadzie i Australii, a WHO ostrzega przed jego globalizacją.
Japonia – dzięki restrykcyjnym regulacjom – uniknęła masowej fali uzależnień, ale równocześnie stała się miejscem intensywnych poszukiwań alternatyw, które pozwoliłyby leczyć ból bez ryzyka uzależnienia. Teraz naukowcy z Uniwersytetu w Kioto opracowali lek, który może odwrócić bieg historii medycyny bólu. ADRIANA – pierwszy selektywny antagonista receptora α2B-adrenoreceptora – działa zupełnie inaczej niż opioidy, zapewniając silne działanie przeciwbólowe bez uzależnienia, depresji oddechowej czy sedacji. Wchodząc w kolejną fazę badań klinicznych, ma szansę stać się nowym złotym standardem leczenia bólu przewlekłego i pooperacyjnego. Wyniki opisano w PNAS.
Receptory α2 – ukryty cel w terapii bólu
Rodzina receptorów adrenergicznych α2, obejmująca podtypy α2A, α2B i α2C, należy do receptorów sprzężonych z białkiem G, które reagują na noradrenalinę i adrenalinę. W warunkach fizjologicznych odpowiadają za regulację uwalniania neuroprzekaźników, a w sytuacjach zagrożenia, w ramach reakcji “walcz lub uciekaj”, wspierają mechanizmy adaptacyjne, między innymi modulując percepcję bólu.
Czytaj też: Nowy lek uśmierza ból jak opioidy – ale bez ich ciemnej strony
Podtyp α2A, obecny w mózgu i rdzeniu kręgowym, po aktywacji hamuje przewodzenie bodźców bólowych. Receptor α2B, dotąd stosunkowo słabo poznany, związany jest głównie z kontrolą napięcia naczyń krwionośnych oraz z mechanizmami bólu mechanicznego. Z kolei α2C uczestniczy w modulowaniu uwalniania dopaminy i serotoniny, wpływając na procesy neurochemiczne o znaczeniu zarówno dla nastroju, jak i percepcji bodźców.
Dotychczasowe leki działające na receptory α2 – jak deksmedetomidyna – były nieselektywne i aktywowały wszystkie podtypy, co powodowało m.in. silną sedację, bradykardię i spadki ciśnienia krwi. Problemem była też forma podania – większość takich preparatów wymagała wlewu dożylnego i nie nadawała się do codziennego, długotrwałego stosowania.
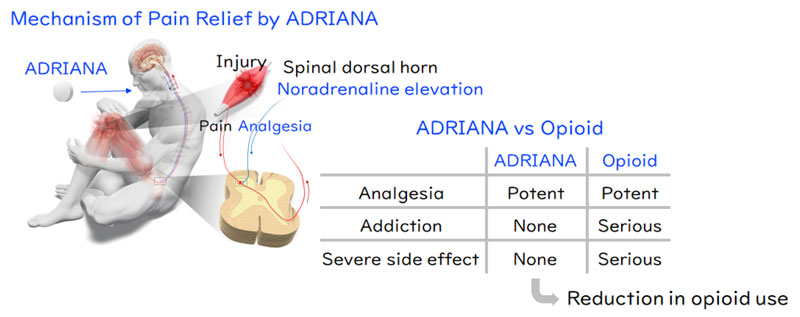
Zespół prof. Masatoshi Hagiwary wysunął hipotezę, że selektywna blokada receptora α2B może pośrednio zwiększyć aktywację receptora α2A poprzez podniesienie poziomu noradrenaliny, co w efekcie doprowadzi do analgezji bez destabilizacji układu krążenia. Aby to potwierdzić, naukowcy musieli znaleźć cząsteczkę, która działałaby wyłącznie na α2B, nie naruszając równowagi w pozostałych podtypach receptorów.
Do tego celu zastosowano zaawansowaną metodę TGFα shedding assay, pozwalającą na niezwykle precyzyjny pomiar aktywności poszczególnych podtypów receptorów adrenergicznych w obecności badanych związków chemicznych. Po szeroko zakrojonych badaniach przesiewowych wyłoniono molekułę nazwaną roboczo c545, a następnie ADRIANA (Adrenergic Inducer of Analgesia). To pierwszy w historii selektywny antagonista receptora α2B.
Pierwszy taki lek na świecie
W modelach zwierzęcych ADRIANA skutecznie redukowała ból neuropatyczny, zapalny i pooperacyjny. W testach obejmujących ligację nerwu rdzeniowego, indukcję zapalenia łapy oraz nacięcie chirurgiczne lek wykazywał efekt porównywalny z morfiną, ale bez sedacji, upośledzenia motoryki czy zaburzeń ciśnienia tętniczego. Wyniki te potwierdzały, że selektywna blokada α2B może być realną alternatywą dla opioidów w wielu typach bólu.
Czytaj też: Produkcja leków biopodobnych w Polsce. „Jurek, to się nie uda!” A jednak udało się
Po badaniach bezpieczeństwa rozpoczęto próby kliniczne w Szpitalu Uniwersyteckim w Kioto. W fazie I, z udziałem zdrowych ochotników, potwierdzono dobrą tolerancję i brak poważnych działań ubocznych. W fazie II, obejmującej pacjentów po operacjach raka płuca, ADRIANA zapewniała skuteczną kontrolę bólu pooperacyjnego, jednocześnie eliminując ryzyko uzależnienia i sedacji. Teraz trwają przygotowania do dużego, wieloośrodkowego badania fazy II w USA, prowadzonego we współpracy z firmą BTB Therapeutics.

W ostatnich latach obserwujemy przełom w medycynie przeciwbólowej – badacze starają się odchodzić od opioidów na rzecz leków celujących w konkretne mechanizmy molekularne. W 2025 r. FDA zatwierdziła suzetriginę – inhibitor kanałów sodowych – jako alternatywę w bólu ostrym. Trwają też prace nad lekami blokującymi kanały wapniowe, modulującymi neuropeptydy (np. substancję P) czy wykorzystującymi immunomodulację w leczeniu bólu neuropatycznego. ADRIANA wyróżnia się na tym tle precyzyjnym, selektywnym działaniem na receptor dotąd uznawany za “farmakologicznie nieuchwytny”.
Znaczenie ADRIANY wykracza poza farmakologię. Jeśli lek spełni pokładane w nim nadzieje, może realnie zmniejszyć liczbę przepisywanych opioidów, a w konsekwencji – liczbę przypadków uzależnienia i zgonów z przedawkowania. Dla USA, gdzie kryzys opioidowy pozostaje nierozwiązany, taka alternatywa miałaby wymiar zarówno medyczny, jak i społeczny.
