15 maja 2024 roku w First Affiliated Hospital of Guangzhou Medical University w Chinach chirurdzy przeszczepili lewe płuco pochodzące od zmodyfikowanej genetycznie świni rasy Bama do klatki piersiowej 39-letniego mężczyzny, który został wcześniej czterokrotnie uznany za zmarłego z powodu braku funkcji mózgu. Zgoda rodziny pozwoliła na przeprowadzenie eksperymentu w warunkach klinicznych, a badanie zostało opisane na łamach Nature Medicine.
Czytaj też: Nowy organ na liście przeszczepów. Historyczna operacja w USA
Organ pochodził od zwierzęcia wyhodowanego w specjalnych, wolnych od patogenów warunkach przez firmę Clonorgan Biotechnology w Chengdu. Płuco poddano sześciu edycjom CRISPR: wyciszono trzy geny kodujące cukry wywołujące natychmiastową odpowiedź immunologiczną, a dodano trzy ludzkie geny związane z regulacją zapalenia i odpowiedzi odpornościowej.
Jak ludzki organizm zareagował na obce płuco?
Najtrudniejsze były pierwsze godziny po operacji – w klasycznych próbach to właśnie wtedy dochodziło do tzw. nadostrego odrzutu, gdy przeciwciała pacjenta oblepiają komórki nowego organu, inicjując zakrzepy i gwałtowny stan zapalny. Tym razem tego scenariusza nie zaobserwowano – co badacze uznali za pierwszy sukces technologii CRISPR w przypadku płuc.
Czytaj też: 48 dni na granicy życia. Wyjątkowy przeszczep w Warszawie
Jednak po dobie zaczęły pojawiać się sygnały odrzutu: produkcja cytokin prozapalnych, napływ leukocytów i widoczny na tomografii obrzęk płucny. Trzeciego dnia odnotowano już klasyczne objawy odrzutu zależnego od przeciwciał (AMR). Do dziewiątego dnia organ nadal funkcjonował, choć z narastającymi uszkodzeniami, aż w końcu na prośbę rodziny eksperyment zakończono.
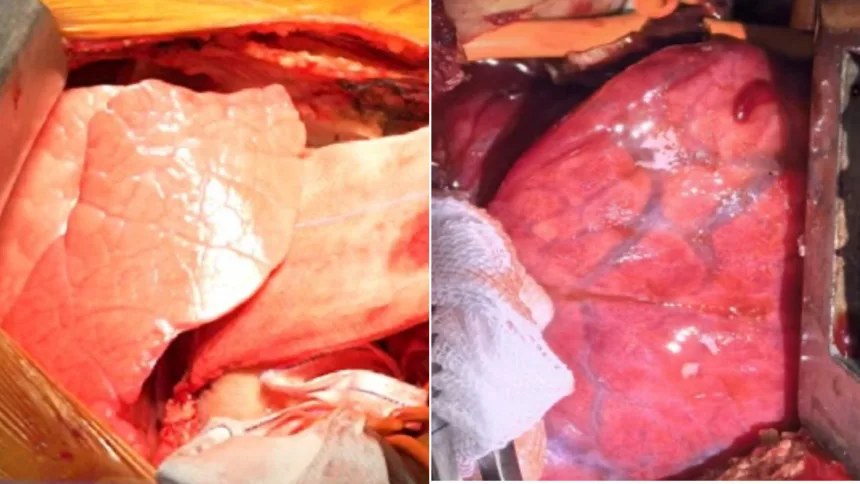
Jiang Shi, współautor badania, mówi:
Dla naszego zespołu to znaczący początek. Ksenotransplantacja płuc stawia unikalne wyzwania biologiczne i techniczne, a naszym celem jest stworzenie naukowej ścieżki do bezpiecznego, trwałego przeszczepu, a nie ogłaszanie gotowości klinicznej.
Płuca to narząd skrajnie delikatny – ich tkanka musi być cienka i przepuszczalna, aby krew mogła wymieniać gazy z powietrzem. Oznacza to jednak, że są ciągle wystawione na działanie bakterii, wirusów, pyłków czy toksyn. Wykształciły więc złożone warstwy obrony immunologicznej, które mogą natychmiast uruchomić stan zapalny.
Ten paradoks – konieczność ciągłej czujności przy jednoczesnej kruchości struktury – sprawił, że przeszczepy płuc od zmarłych dawców zaczęły się udawać dopiero w latach 80. XX wieku – znacznie później niż przeszczepy nerek, wątroby czy serca. Przeniesienie tego doświadczenia na międzygatunkową barierę jest więc jeszcze większym wyzwaniem.
Co dalej?
Światowi liderzy transplantologii podchodzą do wyników z mieszanką entuzjazmu i ostrożności.
Prof. Shaf Keshavjee, torakochirurg i dyrektor Toronto Lung Transplant Program, mówi:
To nie jest jeszcze moment na kliniczne próby. Ważne jest, że badacze pokazali nam, iż wciąż nie jesteśmy gotowi – nie próbujmy tego na żywych pacjentach, bo to się nie uda.
Richard Pierson z Harvard Medical School zwrócił uwagę, że eksperyment miał swoje ograniczenia. Ponieważ pozostawiono prawe płuco pacjenta, trudno było jednoznacznie ocenić, czy świńskie płuco rzeczywiście utrzymywało życie:
Ich wniosek, że mieli funkcjonujące płuco świni, jest nieco optymistyczny. Można było zablokować przepływ krwi do ludzkiego płuca i wtedy realnie ocenić wydolność nowego organu.
Z kolei Luhan Yang, pionierka badań nad eliminacją wirusów PERV z genomu świń, podkreśliła, że mimo wyciszenia antygenów i wprowadzenia inhibitorów układu dopełniacza, nadal dochodziło do silnej odpowiedzi humoralnej:
To wnikliwe badanie, które daje nam cenny wgląd w reakcję immunologiczną wobec płuc świńskich i stanowi punkt odniesienia dla przyszłych postępów w tej dziedzinie.
Co więcej, chiński zespół zastosował bardzo intensywną immunosupresję – ponad pół tuzina leków, by przytłumić odpowiedź odpornościową. Eksperci wskazują, że takie “koktajle” nie są realne u żywych pacjentów, bo prowadziłyby do śmiertelnych infekcji w ciągu dni czy tygodni. Zespół z Guangzhou zapowiedział kolejne eksperymenty na pacjentach w stanie śmierci mózgowej, które mają zweryfikować odpowiednie modyfikacje, m.in. testy przeszczepów obustronnych płuc, wprowadzenie dodatkowych edycji genetycznych czy opracowanie precyzyjniejszych terapii immunomodulujących, np. tymczasowego blokowania przeciwciał, by dać organizmowi “okno tolerancji”.
Czytaj też: Świńskie organy nie pasują do ludzi. Już wiemy, dlaczego
Według danych Global Observatory on Donation and Transplantation w 2024 roku na świecie wykonano 8236 przeszczepów płuc – o 6 proc. więcej niż rok wcześniej. Wciąż jednak dziesiątki tysięcy pacjentów czekają na organ, a wielu z nich nigdy się go nie doczeka. Ksenotransplantacja, obok rozwoju sztucznych i bioinżynieryjnych organów, to jedno z nielicznych rozwiązań, które mogłoby tę lukę wypełnić.
